আজকে আমরা রাদারফোর্ডের পরমাণু মডেল আলোচনা করবো। যা বাউবি এইচএসসি ২৮৭১ পদার্থ বিজ্ঞান ২য় পত্র ইউনিট ৯ নিউক্লিয় পদার্থবিজ্ঞান এর অন্তর্ভুক্ত।
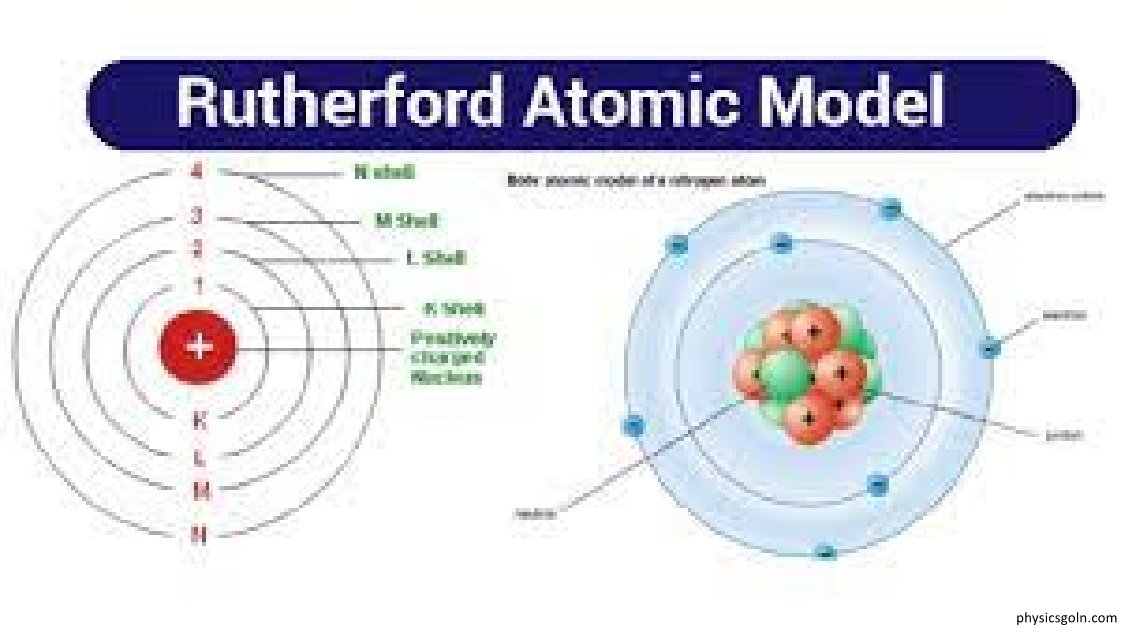
রাদারফোর্ডের পরমাণু মডেল
রাদারফোর্ডের আলফা কণা পরীক্ষা :
1911 সালে রাদারফোর্ডের এবং তাঁর সহযোগী বিজ্ঞানীগণ আলফা কণার বিক্ষেপণ পরীক্ষাটি সম্পন্ন করেন- তেজস্ক্রিয় উৎস থেকে নির্গত a-কণাগুলো সমশক্তি সম্পন্ন হয়। এই a-কণার স্রোতকে সমাাল করে একটি ভারী সোনার পাতলা পাতের উপর ফেলা হয়। সোনার পারমাণবিক সংখ্যা 79। তাছাড়া সোনার পাতকে পিটিয়ে খুব পাতলা, প্রায় 10 m পুরত্বের পাতে পরিণত করা যায়। এর বেধ এত কম হওয়ায় ধরে নেয়া হয় যে, প্রতিটি α-কণা পাতের মধ্যস্থ একটি মাত্র পরমাণুর সাথে সংঘাত বা অজ্ঞক্রিয়া ঘটে।
α-কণা পাতের মধ্য দিয়ে অতিক্রম করার পর বিভিন্ন 8 কোণে বিক্ষিপ্ত হয়। ৪ কোণে বিক্ষিপ্ত α – কণাগুলোকে শনাক্তকরণের জন্য (৯.২) নং চিত্র অনুসারে সোনার পাতকে ঘিরে একটি প্রতিপ্রভ পর্দা রাখা হয়। এই প্রতিপ্রভ পর্দায় -কণা এসে পড়লে পর্দায় একটি আলোর ঝলক দেখা যায়। কোনো কোনো α-কণা সোনার পাতকে অতিক্রম না করে বিক্ষেপের পর আবার আগের অঞ্চলে ফিরে আসে। সেক্ষেত্রে 6 – এর মান 90° অপেক্ষা বেশী হয়।
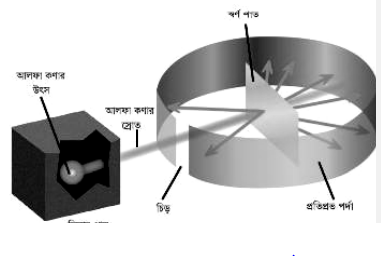
রাদারফোর্ড পরীক্ষার প্রাপ্ত ফলাফলঃ
১। বেশীরভাগ ∝ -কণাই স্বর্ণপাত ভেদ করে সরাসরি বিপরীত দিকে বেরিয়ে আসে কিংবা খুব সামান্যই বিক্ষেপণ ঘটে। α এটি থমসন মডেল দিয়ে ব্যাখ্যা করা যায় না ।
২। অল্প কিছু সংখ্যক α কণা 90° কোণে বা তার চেয়ে কম কোণে বিক্ষিপ্ত হয়।
৩। অতি অল্প কিছু সংখ্যক α – কণা 90° কোণের চেয়ে বেশী কোণে বিক্ষিপ্ত হয়। দেখা গেছে প্রতি 8000 এ একটি α – কণা 90° কোণের চেয়ে বেশী কোণে বিক্ষিপ্ত হয়। কোনো কোনো সময় দেখা যায় একটি α – কণা 180° কোণে বিক্ষিপ্ত হয় অর্থাৎ কণাটি যে পথে যায় সে পথেই ফিরে আসে। মনে হয় যেন স্বর্ণপাতের পরমাণুর সাথে α – কণার মুখমুখী সংঘর্ষ হয়েছে। এটি সে সময়ে বিস্ময়কর ঘটনা ছিল। এটি থমসন মডেল দিয়ে ব্যাখ্যা করা যায় না।
৪। যদি α -কণা তার গতি পথের সাথে φ কোণে বিক্ষিপ্ত হয় এবং সেই বরাবর N সংখ্যক α -কণা আপতিত হয় তবে দেখা গেছে,
1/sin 4φ/2 ∝ loge N সমীকরণটি মেনে চলে ।
৫। যদি পাতের পুরত্ব t হয় এবং N সংখ্যক α -কণা φ কোণে বিক্ষিপ্ত হয় তবে দেখা গেছে, N/t = ধ্র“ব সংখ্যা।
রাদারফোর্ড পরীক্ষার সিদ্ধাড়
১। অধিকাংশ x -কণাই স্বর্ণপাত ভেদ করে সরাসরি বিপরীত দিকে বেরিয়ে আসে। এর থেকে সিদ্ধাড় নেয়া যায় যে, পরমাণুর মধ্যে অধিকাংশ স্থানই শূন্য।
২। কিছু সংখ্যক ∝ -কণা অতি সামান্য বিক্ষিপ্ত হয়। এক্ষেত্রে 0 ≈ 1° অর্থাৎ বিক্ষেপ কোণ 1° এর কাছাকাছি। একে স্বল্প কোণে বিক্ষেপ বলে। এই ঘটনাটিকে a -কণা এবং ইলেকট্রনের মধ্যে কুলম্বীয় আকর্ষণ বলের ফলাফল বলে ধরে নেয়া α যায়। α -কণার চার্জ + 2e এবং ইলেকট্রনের চার্জ -e ফলে স্থির তড়িৎ কুলম্বীয় আকর্ষণ ক্রিয়া করে। যেহেতু α – কণার ভর ইলেকট্রনের ভরের প্রায় 7000 গুণ তাই এই আকর্ষণ বলের কারণে a -কণা অতি সামান্যই বিক্ষিপ্ত হয়। এর থেকে সিদ্ধাড় নেয়া যায় যে, পরমাণুর মধ্যে ইলেকট্রনগুলো বিচ্ছিন্ন ভাবে অবস্থান করে।
৩। অতি অল্প সংখ্যক α – কণা 90° কোণের চেয়ে বেশী কোণে বিক্ষিপ্ত হয়। কোনো কোনো সময় দেখা যায় একটি a- কণা 180° কোণের বিক্ষিপ্ত হয় অর্থাৎ কণাটি যে পথে যায় সে পথেই ফিরে আসে। এর অর্থ হলো, যে সব α – কণা ধনাত্মক চার্জের খুব কাছ দিয়ে গেছে সেই সব α – কণাগুলো 90° কোণের চেয়ে বেশী কোণে বিক্ষিপ্ত হয়েছে এবং যে সব α -কণা ধনাত্মক চার্জের সাথে সরাসরি সংঘর্ষে লিপ্ত হয়েছে সেগুলো 180° কোণে বিক্ষিপ্ত হয়েছে। এর থেকে রাদারফোর্ড এই সিদ্ধাড়ে উপনীত হন যে, পরমাণুর সমগ্র ধনাত্মক চার্জ এবং প্রায় সমগ্র ভর অতি অল্প পরিসরে কেন্দ্রীভূত থাকে। একে রাদারফোর্ড পরমাণুর নিউক্লিয়াস নাম দেন।
রাদারফোর্ড পরমাণু মডেলঃ
একটি সম্পূর্ণ পরমাণুর মধ্যে অতি অল্প পরিসরে বেশী ভর ও ধনাত্মক চার্জ বিশিষ্ট নিউক্লিয়াস এবং বাকি বিশাল অঞ্চল জুড়ে শূন্যস্থান যেখানে বিক্ষিপ্ত ভাবে ঋণাত্মক চার্জযুক্ত ইলেকট্রন ছড়িয়ে আছে। ধনাত্মক চার্জ বিশিষ্ট নিউক্লিয়াসের কাছে এই ভাবে ঋণাত্মক চার্জযুক্ত ইলেকট্রন থাকতে পারে না কারণ এখানে স্থির তড়িৎ কুলম্বীয় আকর্ষণ ক্রিয়া করছে। তাই রাদারফোর্ড পরমাণুকে সৌরমন্ডলের সাথে তুলনা করলেন।
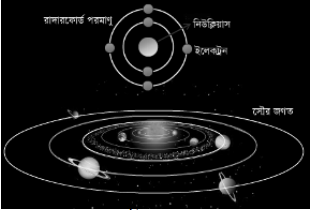
সৌরমন্ডলে যেমন অধিকাংশ অঞ্চলই ফাঁকা স্থান। সূর্যে অল্প পরিসরে সৌরমন্ডলের অধিকাংশ ভরই কেন্দ্রীভূত আছে। গ্রহগুলো বিচ্ছিন্নভাবে সূর্যের চারিদিকে ছড়িয়ে প্রত্যেকে এমন দূরত্বে থেকে আবর্তন করছে যেন গ্রহগুলোর প্রত্যেকের কেন্দ্রমুখী বল ও সূর্যের সাথে তার মহাকর্ষ বল সমান হয়। ঠিক তেমনি নিউক্লিয়াসে অল্প পরিসরে পরমাণুর প্রায় সমড় ভর ও ধনাত্মক চার্জ কেন্দ্রীভূত আছে। ইলেকট্রনগুলো বিচ্ছিন্নভাবে নিউক্লিয়াসের চারিদিকে ছড়িয়ে প্রত্যেকে এমন দূরত্বে থেকে আবর্তন করছে যেন ইলেকট্রনগুলো প্রত্যেকের কেন্দ্রমুখী বল ও নিউক্লিয়াসের সাথে তার কুলম্বীয় বল সমান হয়। এটি প্রকৃতপক্ষে বোরের প্রস্তাব। তাই এ মডেলকে বলা হয় বো- রাদারফোর্ড মডেল। নিম্নে আলোচনা করা হয়েছে ।
রাদারফোর্ড পরমাণু মডেলের সীমাবদ্ধতা ঃ
রাদারফোর্ড পরমাণু মডেলের সীমাবদ্ধতা নিচে দেয়া হলো :
১। ইলেকট্রন নিউক্লিয়াসের চারিদিকে, বৃত্তাকার পথে আবর্তন করছে। সেজন্য ইলেকট্রনের সর্বদা কেন্দ্রমুখী ত্বরণ — আছে। চিরায়ত বলবিদ্যায় ম্যাক্সওয়ের তত্ত্ব অনুসারে ত্বরান্বিত চার্জ তড়িৎচৌম্বক শক্তি বিকিরণ করে। সুতরাং আবর্তনরত ইলেকট্রন অবিচ্ছিন্ন তড়িৎচৌম্বক তরঙ্গ বিকিরণ করবে।
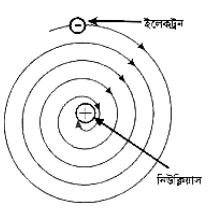
অপর দিকে শক্তি বিকিরণ করলে ইলেকট্রনের মোটশক্তি হ্রাস পাবে ফলে লেখ অনুসারে ইলেকট্রন নিউক্লিয়াসের দিকে এগিয়ে আসবে এবং ইলেকট্রনের বেগ বৃদ্ধি পাবে। এই ভাবে ক্রমান্বয়ে নিউক্লিয়াসের দিকে এগিয়ে গিয়ে নিউক্লিয়াসকে আঘাত করবে ফলে পরমাণুটি ধ্বংস হয়ে যাবে। তাত্ত্বিক গণনায় দেখা গেছে এরকম হলে কোনো পরমাণুর আয়ু 10’s এর বেশী হত না।
সুতরাং রাদারফোর্ড পরমাণু মডেলে পরমাণু অস্থায়ী। কিন্তু বাড়বে বস্তুর স্থায়িত্ব প্রমাণ করে পরমাণু অস্থায়ী নয় । ২। ইলেকট্রন যদি অনবরত শক্তি বিবিরণ করতে থাকে তবে ইলেকট্রনের বেগ বৃদ্ধি পাবে। ফলে প্রতি মূহুর্তে ইলেকট্রনের পর্যায়কাল কমতে থাকবে এবং কম্পাঙ্ক বাড়তে থাকবে।
ক্রমান্বয়ে কম্পাঙ্ক বৃদ্ধির ফলে ইলেকট্রন সকল তরঙ্গ দৈর্ঘ্যের তরঙ্গের বিকিরণ করবে অর্থাৎ পরমাণু থেকে নিরবিচ্ছিন্ন বর্ণালী পাওয়া যাবে। কিন্তু হইড্রোজেন, হিলিয়াম ইত্যাদি মৌলের পরমাণবিক বর্ণালীগুলো হলো রেখা বর্ণালী। নিরবিচ্ছিন্ন নয়।
সার-সংক্ষেপ :
রাদারফোর্ড পরমাণু মডেল :
নিউক্লিয়াসে অল্প পরিসরে পরমাণুর প্রায় সমড় ভর ও ধনাত্মক চার্জ কেন্দ্রীভূত আছে। ইলেকট্রনগুলো বিচ্ছিন্নভাবে নিউক্লিয়াসের চারিদিকে ছড়িয়ে প্রত্যেকে এমন দূরত্বে থেকে আবর্তন করছে যেন ইলেকট্রনগুলো প্রত্যেকের কেন্দ্রমুখী
বল ও নিউক্লিয়াসের সাথে তার কুলম্বীয় বল সমান হয়। |
রাদারফোর্ড পরমাণু মডেলর সীমাবদ্ধতা :
১। চিরায়ত বলবিদ্যায় ম্যাক্সওয়েলের তত্ত্ব অনুসারে ত্বরান্বিত চার্জ তাড়িতচৌম্বক শক্তি বিকিরণ করে। সুতরাং আবর্তনরত ইলেকট্রন অবিচ্ছিন্ন তাড়িতচৌম্বক তরঙ্গ বিকিরণ করবে। অপর দিকে শক্তি বিকিরণ করলে ইলেকট্রনের মোটশক্তি হ্রাস পাবে ফলে ইলেকট্রন নিউক্লিয়াসের দিকে এগিয়ে আসবে এবং ইলেকট্রনের বেগ বৃদ্ধি পাবে।
এই ভাবে ক্রমান্বয়ে নিউক্লিয়াসের দিকে এগিয়ে গিয়ে নিউক্লিয়াসকে আঘাত করবে ফলে পরমাণুটি ধ্বংস হয়ে যাবে। সুতরাং রাদারফোর্ড পরমাণু মডেলে পরমাণু অস্থায়ী। কিন্তু বাড়বে বস্তুর স্থায়িত্ব প্রমাণ করে পরমাণু অস্থায়ী নয়।
বহুনির্বাচনী প্রশ্নঃ
১। আলফা কণা বিকিরণ পরীক্ষা দ্বারা রাদারফোর্ড পরমাণুতে কীসের উপস্থিতির ব্যাখ্যা প্রদান করেন?
ক. ইলেকট্রন
খ. প্রোটন
গ. নিউক্লিয়াস
ঘ. নিউট্রন
২। রাদারফোর্ডের আলফা কণা পরীক্ষা সোনার পাত ব্যবহার করা হয় কারণ
i. সোনার পাতকে পিটিয়ে খুব পাতলা, প্রায় 107m পুর—ত্বের পাতে পরিনত করা যায়।
ii. প্রতিটি o-কণা পাতের মধ্যস্থ একটি মাত্র পরমাণুর সাথে সংঘাত বা অজ্ঞক্রিয়া ঘটে।
iii. সোনার পারমাণবিক সংখ্যা 79, যা আলফা কণার চেয়ে অনেকগুণ ভারী।
নীচের কোনটি সঠিক?
ক. i ও ii
খ. ii ও iii
গ. i ও iii
ঘ. i, ii ও iii
